- Nukleo
- Fizyka
- Biologiczne skutki promieniowania jonizującego
- Wpływ promieniowania na zdrowie
Wpływ promieniowania na zdrowie
Duże dawki promieniowania są zawsze szkodliwe, natomiast małe dawki mogą dawać efekty korzystne. W zakresie małych dawek uszkodzenia naprawiane są przez stosunkowo silne, indukowane przez promieniowanie komórkowe mechanizmy obronne i naprawcze. Substancje chemiczne, czy inne czynniki wewnątrz- lub zewnątrzkomórkowe, powodują podobne uszkodzenia materiału genetycznego co promieniowanie jonizujące, dzięki temu komórka jest ciągle w stanie “gotowości”, a to stawia ją w korzystnej sytuacji. Jednak w miarę zwiększania mocy dawki wydajność komórkowych mechanizmów obronnych maleje.
Skutki napromieniowania małymi dawkami
Dział zatytułowany „Skutki napromieniowania małymi dawkami”Napromienienie ciała małymi dawkami (poniżej 0,2 Sv), które rozłożone są w czasie, może przyczynić się do zwiększenia siły odpowiedzi immunologicznej, ale już zastosowanie większej dawki może przynieść działanie negatywne. Jako przykład można tutaj podać ludność Nagasaki, która została napromieniona dawką ok. 0,1 Sv. W przypadku tej populacji zaobserwowano zmniejszenie zapadalności na białaczki, raka płuc i raka jelita grubego. Takie działanie promieniowania jonizującego wykorzystuje się w terapii, polegającej na ekspozycji całego ciała lub jego połowy 3 razy w tygodniu przez 5 tygodni na działanie dawki ok. 0,1 Gy. Taki rodzaj leczenia może być stosowany jako metoda uzupełniające w leczeniu np. nowotworów.
Oczywiście istnieje koncepcja, że zbyt małe napromienienie organizmu jest szkodliwe. Jeżeli komórka znajdzie się w sytuacji niedoboru czynników stresujących, to może dojść do zmniejszenia sprawności jej mechanizmów obronnych i nie będzie w stanie reagować na małe zagrożenia. Taki mechanizm jest prawdziwy w odniesieniu do wybranych tkanek, jednak ciągle wymaga szerszych badań. Jak pisano wcześniej, różne komórki, a co za tym idzie tkanki i narządy, charakteryzują się większą lub mniejszą promienioczułością i dlatego
Napromieniowanie dużymi dawkami, skutki deterministyczne, choroba popromienna, skutki stochastyczne
Dział zatytułowany „Napromieniowanie dużymi dawkami, skutki deterministyczne, choroba popromienna, skutki stochastyczne”Skutki napromieniowania ciała dużymi dawkami, powyżej 1Sv, są dobrze znane. Wiadomo, że im większa dawka tym większe uszkodzenia. Mniejsze dawki uszkadzają tylko te tkanki, które charakteryzują się większą promieniowrażliwością, natomiast duże dawki uszkadzają wszystkie tkanki lub ich większość. Poniższy rysunek przedstawia biologiczne skutki promieniowania jonizującego.
Skutki deterministyczne
Dział zatytułowany „Skutki deterministyczne”Skutki deterministyczne są to następstwa nieodwracalnego spadku liczby komórek poniżej poziomu niezbędnego do funkcjonowania szczególnie ważnych tkanek i narządów, które w stosunkowo krótkim czasie, po przekroczeniu OKREŚLONEJ DAWKI PROGOWEJ (patrz rysunek poniżej) pojawiają się u wszystkich napromienionych osób. Przykłady dawek progowych dla niektórych skutków deterministycznych indukowanych przez promieniowanie X lub gamma podaje tabela poniżej.
| Skutek | Dawka progowa [Gy] |
|---|---|
| Ostry zespół szpikowy | 1 |
| Trwała niepłodność u mężczyzn | 2,5 - 6 |
| Trwała niepłodność u kobiet | 3,5 - 6 |
| Zmętnienie soczewki oka | 0,5 - 2 |
| Zaćma oczna | 5 |
| Rumień skóry | 3 |
| Sączące złuszczanie naskórka | 20 |
| Martwica skóry | 50 |
| Powstawanie wad rozwojowych płodu | 0,1 - 1 |
Ostra choroba popromienna
Dział zatytułowany „Ostra choroba popromienna”Ostra choroba popromienna to zespół zmian ogólnoustrojowych występujących po napromieniowaniu całego organizmu (lub większej jego części) dużą dawką, poczynając od LD50/30 (dawka śmiertelna). W zależności od wielkości dawki (patrz poniższa tabela), po okresie tzw. zwiastunów (przed dojściem do pełnego obrazu choroby) z nudnościami i wymiotami, pieczeniem poparzonej skóry, na pierwszy plan wysuwają się objawy:
- ostry zespół szpikowy (szpik kostny) - w wyniku zniszczenia szpiku kostnego stale maleje we krwi ilość elementów morfotycznych (białe ciałka krwi, czerwone ciałka krwi i płytki krwi), występują krwotoki i załamanie odporności organizmu;
- ostry zespół jelitowy (nabłonek przewodu pokarmowego) - do objawów uszkodzenia szpiku kostnego dochodzą objawy ostrego zapalenia śluzówki jelit (brak łaknienia, senność, wysoka temperatura i biegunka prowadząca do odwodnienia organizmu);
- ostry zespół Centralnego Układu Nerwowego (CUN) - śródbłonek naczyń krwionośnych w mózgu; pierwszymi objawami są pobudzenie naprzemiennie z apatią, utrata równowagi i zaburzenie koordynacji ruchowej, drgawki i śmierć wśród innych pozostałych objawów ostrej choroby popromiennej. Przyczyną zgonu jest obrzęk mózgu i wzrost ciśnienia wewnątrzczaszkowego.
| Dawka [Gy] | Rodzaj zespołu | Śmiertelność [%] |
|---|---|---|
| 1-10 | Ostry zespół szpikowy | 0-9 |
| 10-50 | Ostry zespół jelitowy | 90-100 |
| >50 | Ostry zespół CUN | 100 |
Skutki stochastyczne
Dział zatytułowany „Skutki stochastyczne”Skutki stochastyczne działania promieniowania na organizm człowieka, to następstwa, które z dużym opóźnieniem czasowym ujawniają się tylko u niektórych osób z ogółu napromienionych. Nie można jednak przewidzieć, u której spośród osób napromienionych taką samą dawką, następstwa te wystąpią, a jeśli wystąpią, to czy na pewno z powodu działania promieniowania.
Przykłady skutków stochastycznych:
- zwiększenie prawdopodobieństwa wystąpienia jednej ze znanych chorób nowotworowych u osoby napromienionej,
- zwiększenie prawdopodobieństwa wystąpienia jednej ze znanych wad lub chorób dziedzicznych u potomstwa napromienionej osoby.
Różnice pomiędzy skutkami deterministycznymi i stochastycznymi przejawiają się we wpływie dawki na częstotliwość (prawdopodobieństwo) ich występowania oraz ostrość wywołanych objawów chorobowych. Po przekroczeniu dawki progowej wzrost dawki powoduje gwałtowny wzrost częstotliwości skutków deterministycznych.
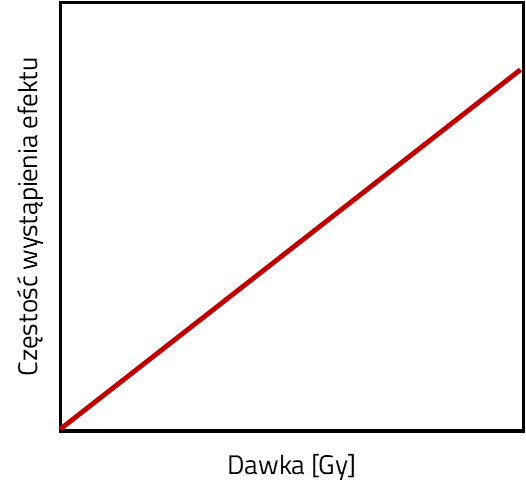
Charakterystyczną cechą skutków deterministycznych jest to, że ich ostrość rośnie wraz ze wzrostem dawki promieniowania. Ostrość skutków stochastycznych nie zależy od dawki, chociaż prawdopodobieństwo ich wystąpienia rośnie wraz ze wzrostem wielkości dawki efektywnej (patrz rysunek poniżej). Skuteczna ochrona przed deterministycznymi skutkami dużych dawek promieniowania polega na ograniczeniu dawek pochłoniętych do wartości niższych od wartości dawek progowych. Ochrona przed stochastycznymi skutkami promieniowania opiera się na zmniejszeniu prawdopodobieństwa ich występowania do najniższego poziomu osiągalnego przy rozsądnym uwzględnieniu czynników ekonomicznych i społecznych.
Działanie promieniowania na zarodek i płód
Dział zatytułowany „Działanie promieniowania na zarodek i płód”W okresie wczesnej ciąży napromienienie dużą dawką prowadzi najczęściej do śmierci zarodka, ponieważ ludzki zarodek/płód jest bardziej promieniowrażliwy niż dorosły człowiek.
- Od 2 do 8 tygodnia ciąży może dojść do wzrostu częstości występowania wad rozwojowych narządów i części ciała.
- Od 8 do 15 tygodnia ciąży - wzrost częstości zmian strukturalnych mózgu, które będą powodować niedorozwój umysłowy różnego stopnia.
- W drugiej połowie 2 trymestru i w 3 trymestrze ciąży promieniowanie nie powoduje już anomalii rozwojowych, a jedynie zwiększa ryzyko zachorowania na białaczkę przed 10 rokiem życia.
Dziedziczne skutki promieniowania
Dział zatytułowany „Dziedziczne skutki promieniowania”Około 13% wszystkich żywo urodzonych dzieci wykazuje mniej lub bardziej poważne naturalne wady i choroby dziedziczne. Przyczyną pierwszych są dominujące, recesywne i dziedziczone w związku z płcią, mutacje genowe w komórkach rozrodczych jednego lub obojga rodziców. Choroby dziedziczne są następstwami wieloczynnikowymi, co oznacza, że wymagają zmutowania nie jednego, ale wielu genów warunkujących wystąpienie danego zaburzenia.
U potomstwa napromienionych osób nie stwierdzono, jak dotąd, występowania żadnych skutków dziedzicznych, mimo że napromienienie ludzkich komórek rozrodczych prowadzi do powstania w nich mutacji.
Przypuszczalnie dla tego typu następstw zależność dawka – skutek ma charakter progowy i stąd wywołanie ich przez dawki mniejsze od 1 Gy nie powinno nastąpić.
Rakotwórcze działanie promieniowania
Dział zatytułowany „Rakotwórcze działanie promieniowania”Za przyczynę skutków stochastycznych przyjmuje się mutacje w komórkach macierzystych. Wiadomo, że nowotwory popromienne są jedynym rodzajem skutków stochastycznych u ludzi i pojawiają się z dużym opóźnieniem czasowym, nazywanym okresem utajenia. Najkrótszy okres utajenia występuje w przypadku białaczek i wynosi dwa lata. W przypadku innych rodzajów nowotworów czas utajenie może sięgać nawet 30 lat.
Promieniowanie nie wywołuje żadnego charakterystycznego nowotworu, a jedynie zwiększa prawdopodobieństwo występowania tych, które z większą lub mniejszą częstością pojawiają się w całej populacji. Oczywiście podatność na choroby nowotworowe wywołane promieniowaniem jonizującym zależy od wielu czynników, takich jak: obszar napromienionego ciała, wiek, płeć. Jak już wspominano, miejsca ciała, w których znajdują się narządy krytyczne czy komórki silnie namnażające się, są bardziej podatne na rozwój nowotworu. Należy też mieć na uwadze, że taka sama dawka zaabsorbowanego promieniowania może spowodować wystąpienie nowotworu u jednego osobnika, a u drugiego już nie.
W tej sytuacji nie jest rzeczą możliwą wskazanie, który nowotwór został wywołany przez napromieniowania, a który przez inne czynniki rakotwórcze znajdujące się w środowisku.
Przy analizowaniu wpływu promieniowania jonizującego na organizm ludzki należy też mieć na uwadze to, że radionuklidy po wchłonięciu do organizmu są z niego wydalane. Z tego względu, oprócz okresu połowicznego zaniku danego izotopu, należy wziąć pod uwagę tzw. biologiczny okres połowicznego zaniku, czyli czas po którym w wyniku procesów biologicznych pozostaje w organizmie średnio połowa pochłoniętego radionuklidu. Biologiczny okres połowicznego zaniku może być o wiele rzędów wielkości krótszy od fizycznego okresu połowicznego zaniku (np. okresy zaniku dla trytu H-3 wynoszą: „biologiczny”: 10 dni, „fizyczny”: 12,3 lat). Do organizmu mogą też dostać się takie radionuklidy, których „biologiczny” okres połowicznego zaniku jest dłuższy, niż przeciętny czas trwania danego izotopu (np. Sr-90 trwale osadza się w kościach).